研究内容
バイオ医薬品の中の抗体医薬品
我々の主な研究対象としているバイオ医薬品は、抗体医薬品です。この抗体医薬品の分野は、この二十年で急速に成長し、世界の医薬品売上高のトップ10のうち、7つを抗体医薬品が占めるまでになっています。抗体医薬品は、すでに、ガンや自己疾患、感染症などの様々な疾患に対する治療薬として医療の現場で使用されていますが、現在も、数多くの新しい抗体医薬品が、世界中で開発されています。
何故、このように抗体医薬品が注目されるのでしょうか。抗体はそもそも、我々の体を様々な病原体から守る免疫系の中の重要な分子として機能しています。その機能は、抗原(病原体などの抗体の標的をいう)に特異的に結合し、排除する役割を持ったタンパク質分子です。そのため、抗体医薬品は、その高い分子標的能により、高い薬効を発揮することのできる医薬品になるのです。さらに、この抗体は、医薬品として重要ないくつかの作用機序を持っていることも、抗体が医薬品として有望である理由です(図参照)。
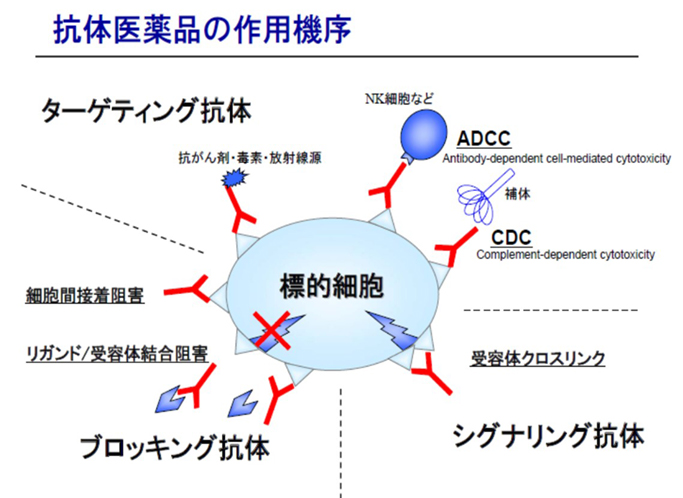
我々の研究は、この抗体を更に高機能化することで、今まで適用できなかった病気の治療に役立てる研究をしています。1つだけ例を挙げましょう。今まで、脳の病気には、抗体医薬品は使用できないか、使用しても極めて効果が低いと考えられてきました。これは、血液に投与した抗体は、脳血液関門(Blood Brain Barrier)のために、ごくわずかしか脳に移行できず、その効果が期待できないことが理由です。そこで、私たちは、独自で開発したAccumuBrainという高機能化技術を使って、脳に抗体を通常の50倍以上も移行させることに成功しました。現在、この技術を使って、アルツハイマー病等の脳疾患に対する抗体医薬品の開発が進められています。このようなバイオ医薬品の開発は、治療効果のある抗体に、別の機能性分子を連結し、抗体を高機能化することで達成されます。私たちは、このようのコンセプトの下、新しい高機能性のバイオ医薬品開発に挑戦しています。
これらの研究の支柱となる3つの技術について、説明しましょう。
1. ファージディスプレイ技術
ファージライブラリ:
この技術を確立した、ミズーリ大学のG. Smith教授と、英国MRCのSir G. Winter教授に、2018年のノーベル化学賞が与えられたことは記憶に新しいことと思います。この技術は、簡単に言えば、任意の外来遺伝子を、バクテリアに感染するウイルスであるバクテリオファージ(M13ファージ)のゲノムDNAに組み込んだ組み換え型ファージを作成して、外来遺伝子の産物であるペプチドやタンパク質(抗体を含む)をバクテリオファージの表面に提示する技術です(図参照)。バクテリオファージは、通常、一度に108-12個も取り扱えるので、一個一個のバクテリオファージに異なる遺伝子を入れることで、108-12種類もの多く種類のペプチドやタンパク質を提示した集団(これをライブラリと呼びますが)を作ることができます。
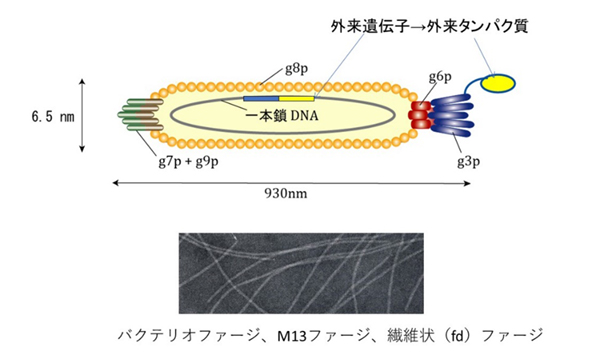
抗体ファージライブラリ、ペプチドファージライブラリ:
我々の体の中には、極めて多くのB細胞がいて、体の中に病原体(異物)が入ってきた際に、これらに結合して中和したり除去したりするための蛋白質である抗体を分泌します。実は、1つのB細胞が分泌する抗体は1種類ですが、様々な外敵に対応するため我々の体には、多様な異なる種類の抗体を分泌できる数多くのB細胞が準備されています。病原体が体内に入ってきた際、いわゆる免疫応答によって、この中から病原体に結合できる抗体を生産できるB細胞が活性化・増殖し、抗体を分泌することで、病原体を排除し、我々は病気から免れることになります。このような多様な抗体の遺伝子を、上述のファージディスプレイ技術によってライブラリ化したものが、抗体ファージライブラリと呼ばれるものです(図参照)。一旦このような抗体ファージライブラリを作っておけば、この中から、標的となる分子に特異的に結合する抗体を、迅速に単離することができます。
抗体の代わりに、ランダムな配列を持つペプチド遺伝子をバクテリオファージ(こちらはT7バクテリオファージを使うことが多いのですが)に導入して、ライブラリ化したものをペプチドファージライブラリと呼んでいます。この中から、多くの機能性をもつペプチドを単離・デザインすることができます。ファージライブラリ法の詳細については、こちらを参照ください。このようにして、単離・デザインした抗体やペプチドを使って、新たなバイオ医薬品開発研究に応用することができます。
2. 抗体部位特異的修飾技術CCAP法(Chemical conjugation by affinity peptide)
我々の研究室では、ペプチドファージライブラリから単離した、IgG抗体のFc領域に特異的に結合するペペプチド(IgG結合ペプチド、IgG-BP)をベースに、IgG抗体を部位特異的に修飾する技術CCAP法を開発しました(図上段)。この技術を使うことで、簡単に、IgG抗体に、他の機能性の分子、例えば、医薬品(抗癌剤)や放射性核種、治療用タンパク質等を容易に連結し、抗体を更に高機能化することで、新たなバイオ医薬品を創製することができます(図下段)。すでに、この技術の応用として、企業の中で実用化研究に進んでいるものもあります。
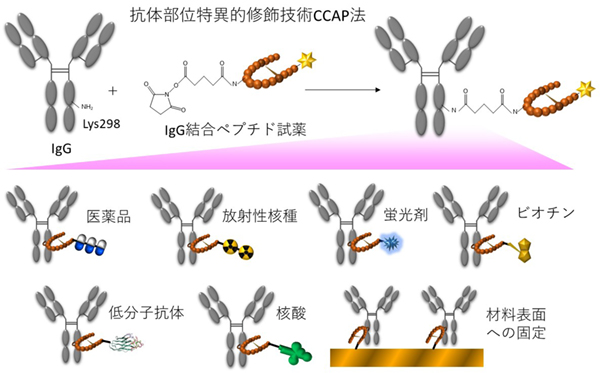
3. 親和性リガンド設計(ペプチド、VHH、単鎖Fv抗体)
ペプチド:
ペプチドというのは、タンパク質と同じようにアミノ酸がつながってできているもののうち、その個数が少ない(通常50個以下)小さなタンパク質ともいえる分子を指します。我々の研究室では、先のペプチドファージライブラリを使って、いくつかの機能性のペプチドを単離しており、すでに、実用化研究を行っているものもあります。
VHH:
アルパカやラクダ、ラマのようないわゆるラクダ科の動物は、我々の持つIgG抗体(IgG1)とは異なるIgG抗体(IgG2, IgG3)を持っています(図参照)。この重鎖抗体と呼ばれる抗体は、我々の持つ重鎖2本と軽鎖2本によるIgGでなく、(CH1領域が欠損している)特殊な重鎖2本のみからなる抗体です。重鎖抗体において最も重要な抗原を認識する抗原結合領域をVHHと呼んでおり、このVHHは、分子が小さくコンパクト(分子量15 kDa)であり、バクテリアで高い生産性を持ち、通常の抗体と同様の抗原認識能を持つだけでなく、ヒト化(ヒトの分子と似せること)も可能です。すでに一部は抗体医薬品として利用されていますが、現在、我々は、ガン細胞や病原性ウイルス、バクテリアを特異的に認識するVHH抗体を単離して、病気の診断と治療薬の開発につなげる研究を進めています。
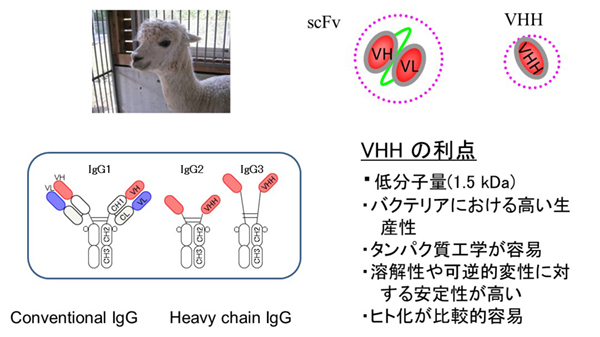
単鎖Fv抗体:
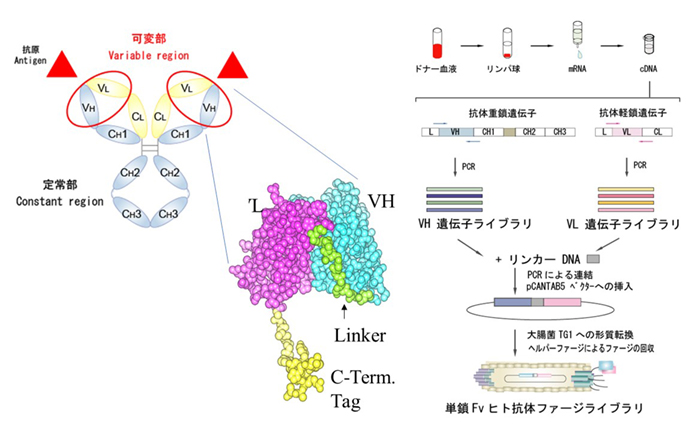
我々のもつIgG抗体は、上述したように、重鎖2本と軽鎖2本から成り立っています。特に抗原を認識する領域、抗原結合領域は、VHとVLという2つのドメイン(鎖)で構成され、Fv領域と呼ばれています。この2つの鎖を、リンカーと呼ばれるものでつないだ分子を単鎖Fv抗体(分子量:25 kDa)と呼んでいます。これは、IgG抗体とほぼ同様な抗原結合能を有するため、IgG抗体の代わりに使用することもできます。一般に抗体ファージライブラリでは、分子量が大きすぎるため、IgG抗体(150 kDa)そのものの提示することはできないので、この単鎖Fv抗体を提示した抗体ライブラリをよく使用します。人の血液由来のB細胞からとってきた抗体遺伝子をもとに、抗体ファージライブラリを構築し、この抗体ファージライブラリから標的に特異的に結合する単鎖Fv抗体を単離すれば、これをもとにIgG抗体に変換して、そのままヒト抗体治療薬として利用することができます。
研究テーマ
- 組織移行性抗体(AccumBodyTM)による標的部位に対する高い志向性を持つバイオ医薬品の開発
- CCAP法を用いた診断・治療用放射性標識抗体医薬品の開発
- 高品質かつ高い安全性を持つ高機能性バイオ医薬品の開発
- ラクダ科(アルパカ、ラクダ)VHH抗体によるガン、感染症に対するバイオ医薬品の開発
- 抗体を用いたガン、感染症に対する高信頼性診断システムの開発
研究プロジェクト
- 2020.4.1 AMED医薬品等規制調和・評価研究事業 「多重特異性抗体等次世代抗体医薬品の品質・安全性評価に関するレギュラトリーサイエンス研究」、研究分担者(2020-2022年度)*実施中
- 2019.10.1 AMED先端的バイオ創薬等基盤技術開発事業 「完全ヒト抗体×ファージライブラリによる組織特異的移行性抗体AccumBodyの開発と次世代複合バイオロジクスへの応用」、研究開発代表者(2019-2023年度)*実施中
- 2018.4.2 AMED医療研究開発革新基盤創成事業「セラノスティクス概念を具現化するための創薬拠点整備を伴う、抗体等標識治療薬(アルファ線)とコンパニオン診断薬の開発」、研究分担者(2018-2021年度)*実施中
- 2014.10.24 AMED革新的バイオ医薬品創出基盤技術開発事業「ヒトIgG特異的修飾技術による多様な機能性抗体医薬の創出」、研究代表者(2014-2018年度)*終了 https://www.amed.go.jp/program/list/06/01/i-biomed/subject/2014/06/index.html
新聞報道等
2020
- ” 特集「低分子抗体の本命はVHH抗体:CAR-T、BBB通過、経口薬も、武田薬品は3種のパイプライン導入」”、日経バイオテク(2020年2月17日)
2019
- ” 微生物で「抗体医薬」安く がんなどの診断・治療 東京農工大など、生産コスト10分の1に”、日本経済新聞(2019年1月21日)
- ” 「オールジャパンでの医薬品創出」プロジェクト公開シンポジウム【午前】:伊東祐二「ヒトIgG特異的修飾技術による多様な機能性抗体医薬の創出」”、YouTube https://youtu.be/psp28ensWMQ (2019年5月7日配信開始)
- 「オールジャパンでの医薬品創出」 プロジェクト 成果報告パンフレット
2018
- ”文科省部会、革新バイオの事業成果を評価、35件の企業への導出など達成”、日経バイオ(2018年12月11日)
- ”進化応用技術ノーベル賞”, 西日本新聞(2018年10月4日)*他、南日本新聞、中日新聞など多数誌にノーベル賞解説記事掲載
- ”オールジャパンでの医薬品創出プロジェクトパンフレット:導出事例”, AMED成果報告 Vo. 1(2018年)
- ”AMED成果報告会 革新的バイオ医薬品創出基盤技術開発事業”, 科学新聞(2018年9月14日、21日)
- ”環状 非天然 多機能カギ”, 化学工業日報(2018年4月10日)
- ” AMED革新的バイオ医薬品創出基盤技術開発事業 平成26、27年度採択27課題紹介”, 科学新聞(2018年3月23日)
- ”「見えてきた成果」5年以内に企業に引き継ぐ”, 科学新聞(2018年2月23日)
2017
- ”ガン抗体薬 品質安定”, 日経産業新聞(2017年4月6日)
- ”日本メジフィジックス 特異部位への抗体標識 鹿児島大から実施権”, 化学工業日報(2017年4月7日)
- ”メジフィジックス 鹿児島大・伊東氏の開発技術で特許契約”, RISFAX(2017年4月7日)
- ”抗体と薬剤の結合制御 病変狙い撃ち技術開発”, 南日本新聞(2017年5月3日)
- “鹿児島大学と日本メジフィジックス 部位特異的抗体標識技術に関する特許の実施に係る契約を締結”、日本メジフィジックス株式会社プレスリリース(記事:鹿児島大学ホームページ、日経バイオテクONLINE、QLifePro 医療NEWS)(2017 年 4 月 6 日)




